¡Felicitamos calurosamente a nuestra División de Productos Polipeptídicos por pasar exitosamente la inspección en sitio de la FDA de EE. UU. con “cero defectos”!
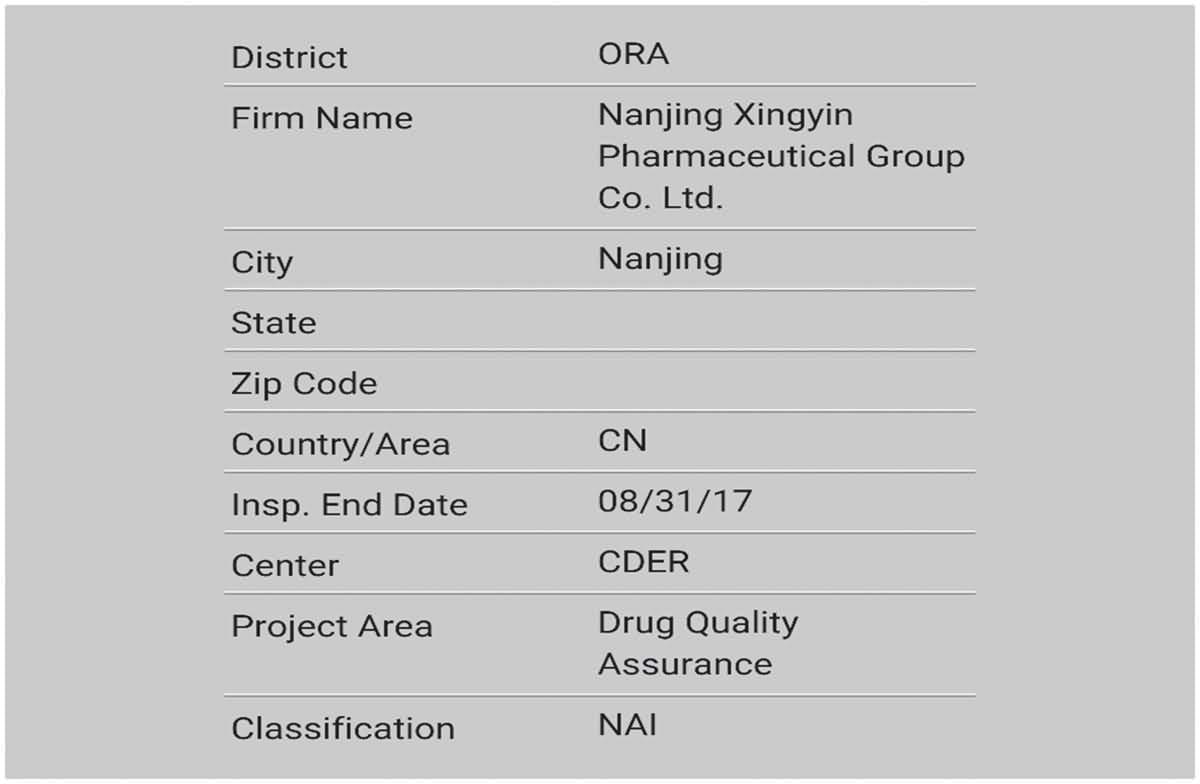
Aprobar la inspección in situ de la FDA con cero defectos es un hito importante en nuestro desarrollo de cGMP. Esto no solo significa que nuestro API ha obtenido la autorización para entrar en el mercado estadounidense, sino que también demuestra que la implementación de cGMP en nuestra empresa se ha alineado gradualmente con los estándares internacionales.
Hora de publicación: 02-mar-2019







